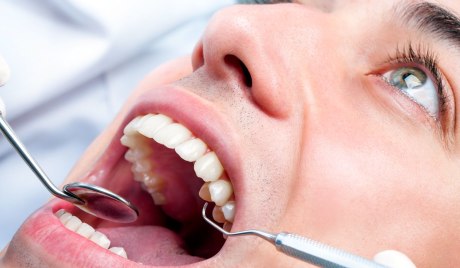
Die Bekanntheit benutzt Lil BUB, um Geld für Tierheime und Tierschutzorganisationen zu sammeln und Katzen in Not zu helfen.
Lil Bub war von Geburt an sehr klein, bereits im Alter von sieben Monaten endete ihr Wachstum. Ihre Schnauze ist verkürzt, ihre Zunge hängt heraus und an jeder Pfote hat sie zusätzliche Zehen. Außerdem wurde bei ihr die „Marmorknochen-Krankheit“ (infantile maligne Osteopetrose) festgestellt, eine seltene Erkrankung, bei der die Knochendichte mit zunehmendem Alter immer weiter zunimmt. Doch gerade diese Eigenheiten haben der Katze im Internet Millionen Follower beschert.
Molekularbiologen aus Deutschland und den USA berichten aktuell, dass eine Kombination von zwei seltenen genetischen Veränderungen die einzigartige Erscheinung der berühmten Katze verursacht. Eine ist für die Entwicklung der zusätzlichen Zehen (Polydaktylie) verantwortlich, die andere für die Knochenerkrankung (Osteopetrose), aus der auch ihre geringe Größe und kurze Schnauze resultieren.
Dr. Darío G. Lupiáñez (Berliner Institut für Medizinische Systembiologie am Max-Delbrück-Centrum für Molekulare Medizin, Berlin), Dr. Daniel Ibrahim (Max-Planck-Institut für molekulare Genetik, Berlin) und Dr. Orsolya Symmons (University of Pennsylvania, Philadelphia, USA) stießen zufällig im Internet auf eins der Videos der Katze. Sie vermuteten, dass Lil Bubs außergewöhnliches Aussehen durch ähnliche genetische Veränderungen verursacht sein könnte wie bei den Patienten sowie den Mäusen, mit denen sie sich beschäftigen.
„Entwicklungsprozesse wie die Knochenbildung sind bei Säugetieren konserviert. Das heißt, sie verlaufen bei allen Arten sehr ähnlich. Die Mutationen zu identifizieren, die Bubs Phänotyp, also ihrem Aussehen zugrunde liegen, könnte uns daher helfen, diese seltenen Erkrankungen auch beim Menschen besser zu verstehen“, sagt Ibrahim. Lil Bubs Besitzer Mike Bridavsky war von der Idee begeistert und stellte den Forschern eine Blutprobe für die Untersuchung zur Verfügung. Anschließend wendeten sich die Wissenschaftler an die Öffentlichkeit und sammelten im Rahmen eines Crowdfunding-Projekts namens „LilBUBome“ mehr als 7.000 Euro.
Die Forscher wollten mit ihrem Projekt nicht nur Lil Bubs Genom analysieren, sondern auch die Möglichkeiten moderner Genetik zeigen. Sie informierten von Anfang an mithilfe eines eigens dafür eingerichteten Blogs und Social Media die Öffentlichkeit über die Fortschritte der Arbeit und die dabei auftretenden Probleme. Dabei lief das Projekt parallel zu den eigentlichen Arbeiten, bei denen die drei Forschenden seltene Erkrankungen beim Menschen und die Regulation von Genen erforschen.
Noch bevor sie das Genom sequenzierten, machten Lupiáñez, Ibrahim und Symmons eine vorbereitende Analyse. Sie stellten fest, dass die zusätzlichen Zehen der Katze durch eine bereits bekannte genetische Variante verursacht wurden, die die Regulation des sogenannten Sonic-Hedgehog-Gens kontrolliert. Eine identische Variante dieses Gens hatten auch die Katzen des Schriftstellers Ernest Hemingway. Sie sind dafür berühmt, dass sie an ihren Vorderpfoten sechs Zehen besaßen.
Etwa fünfzig Nachkommen dieser Katzen leben immer noch im Ernest Hemingway Museum in Key West, Florida. „Das ist sehr aufschlussreich. Lil Bub ist eine Waise, sie wurde als verwildertes Kätzchen im ländlichen Indiana gefunden. Aber obwohl wir keinerlei Informationen über ihre Herkunft haben, gibt uns die in ihrem Genom enthaltene Information Hinweise zu ihrer möglichen Herkunft und zu ihrer entfernten Verwandtschaft“, sagt Symmons. Die genetische Veränderung zu finden, die Lil Bubs Osteopetrose verursacht, dauerte etwas länger: Eine erste Auswertung ihres Erbmaterials ergab etwa sechs Millionen möglicher Unterschiede zwischen ihrem Genom und dem Katzen-Referenzgenom. Normalerweise hätten die Forscher in einem zweiten Schritt Lil Bubs Genom mit dem ihrer gesunden Verwandten verglichen – doch das war in diesem Fall nicht möglich. „Aber wir hatten das große Glück, mit Genetikern zusammenzuarbeiten, die auf Erkrankungen des Skelettsystems beim Menschen spezialisiert sind“, sagt Ibrahim. „Sie haben uns dabei geholfen, die immense Menge an Varianten auf eine überschaubare Zahl an potenziell krankheitsverursachenden Veränderungen zu verringern. Diese konnten wir dann einzeln untersuchen.“ Bei der Analyse dieser Daten fanden die Wissenschaftler heraus, dass eine einzelne Base in einem Gen fehlte, welches bereits zuvor bei Menschen und Mäusen mit Osteopetrose in Verbindung gebracht worden war.
Die Wissenschaftler hoffen jetzt auf Unterstützung weiterer Wissenschaftler, die ihren Erfahrungsschatz und ihre Expertise in das Projekt einbringen. Um Teilnahme am Projekt zu ermöglichen, haben die Forscher ihre Ergebnisse auf der allgemein zugänglichen Pre-Print-Plattform BioRxiv veröffentlicht.